Comment réaliser un plan de complémentation ?
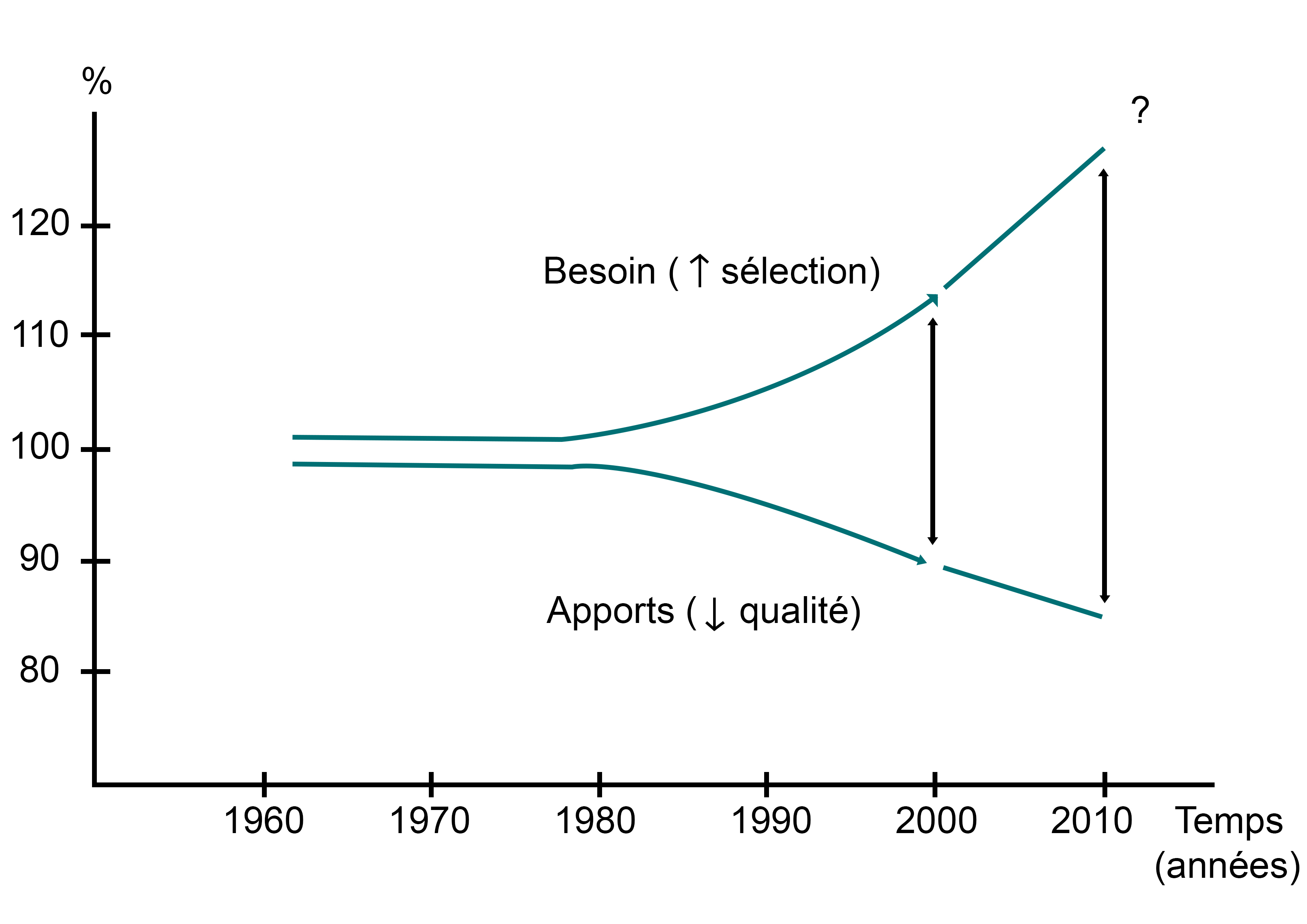
Mise en œuvre pratique d’une complémentation minérale en élevage bovinEn élevage bovin, les évolutions de l’agriculture actuelle (monocultures, sélection de races hyperproductrices, sols carencés…) sont à l’origine d’un écart grandissant entre apports en minéraux et besoins des animaux (figure 8), augmentant ainsi la probabilité d’apparition de carences. Par ailleurs, la meilleure connaissance du rôle des oligo-éléments dans les réactions métaboliques entraine une recherche des carences plus fréquente.
Dans un tel contexte, divers outils permettent au vétérinaire, de recommander à ses éleveurs, des méthodes de gestion des carences ou excès en oligo-éléments au sein de son exploitation.
Evaluation des pratiques alimentaires
Vérification de la ration dans son ensemble
Dans un premier temps, il est important de vérifier la ration dans son ensemble. En effet, lorsque l’origine alimentaire d’un trouble est mise en évidence, il convient de vérifier dans un premier temps les éléments majeurs de la ration tels que les apports en énergie, en fibres, en matière azotée… (Arthington, 2003; Chantreau, 2017). Dans ce cas de figure, il convient de vérifier :
- Le rationnement théorique : c’est-à-dire évaluer les apports calculés pour la ration, mais aussi le système de conception et son adaptation aux stades physiologiques et aux besoins des animaux de l’élevage.
- La qualité de la ration distribuée : c’est à dire la quantité de fourrages distribués et la composition en minéraux de ces fourrages.
- La quantité de ration réellement ingérée : en fonction des phénomènes de dominance, des parties de la ration sont « triées » par les bovins et non consommées.
- La partie réellement valorisée de la ration, c’est-à-dire quelles sont les performances des bovins par rapports à celles théoriquement attendues avec la ration qu’ils reçoivent (Wolter & Ponter, 2013).
Cette même analyse devrait être réalisée lors de suspicion de carence en oligo-éléments. Cependant, cela est rarement fait compte tenu du prix des analyses. C’est la comparaison des quantités distribuées dans la ration et des apports journaliers recommandés qui permet de mettre en évidence les insuffisances de la ration (Guerin, 2010).
Enfin, il a été montré que la très grande majorité des rations distribuées aux ruminants sont déficitaires en minéraux. Cela est d’autant plus marqué pour les oligo-éléments. Il est donc parfois possible de s’intéresser directement à la complémentation en minéraux sans analyser les fourrages (Rollin, 2002).
Les objectifs d’une complémentation minérale sont de :
- Corriger une carence avérée et réduire les signes cliniques associés,
- Couvrir les besoins optimums en santé, bien-être et productivité des animaux,
- Eviter les excès (Rollin, 2016).
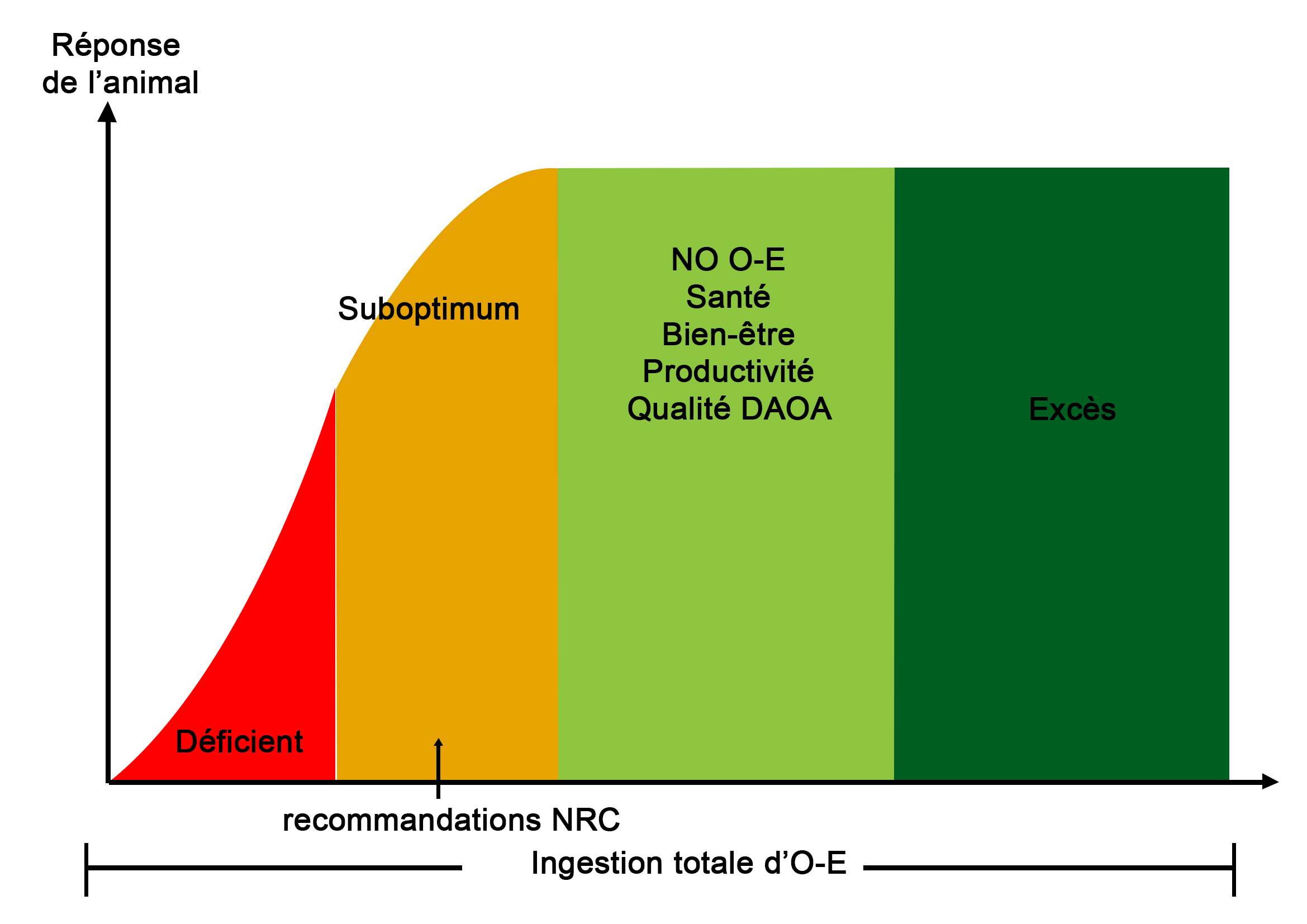
Pour cela, des recommandations émises par l’INRA ou encore le NRC existent.Les normes INRA par exemple ont été émises en 1988 et revues en 2010 et incluent une marge de sécurité afin de limiter au maximum les possibilités de dépasser les seuils de toxicité. En effet, certains oligo-éléments ont une action toxique lorsqu’ils sont absorbés en trop grande quantité. Par exemple, lors d’excès de cuivre, une accumulation hépatique de l’élément s’opère suivie d’une libération brutale dans la circulation sanguine. Cela peut entrainer une destruction des globules rouges et une nécrose rénale. De même, le fer, l’iode et le sélénium sont toxiques car ce sont des oxydants puissants (Meschy, 2010). Ainsi, les apports recommandés se situent entre les seuils de carence et de toxicité pour les oligo-éléments et souvent ils sont inférieurs aux quantités optimales pour la santé, le bien-être et la productivité, afin de garder une marge par rapport aux seuils de toxicité (cf figure ci-contre).
Il est important de noter que ces recommandations sont globalement faibles, ne permettant à l’animal d’atteindre qu’un sub optimum en terme de bien-être et productivité.
Ces normes varient en fonction de certains paramètres et, comme le montre la figure ci-dessus, ils sont relativement bas par rapport aux besoins de production des animaux (Rollin, 2016) :
- Biodisponibilité des minéraux considérés (forme organique ou inorganique, possibilité d’interaction ou non)
- Productivité des animaux, stress
- Capacité d’ingestion (baisse en fin de gestation)
Les recommandations doivent servir de base pour le calcul de la complémentation par rapport à la ration. Ils sont néanmoins propres à chaque élevage, suivant la ration utilisée et la qualité de celle-ci, surtout vis-à-vis des oligo-éléments. Il est aussi important d’adapter les quantités d’apports en fonction de la présence ou non de certaines substances dans la ration, comme des produits goitrogènes, des thiomolybtates, des nitrates, un éventuel déficit en acides aminés de la ration… (Pin, 2007).
Les carences en oligo-éléments peuvent être de deux sortes :
- Les carences primaires, qui correspondent à une consommation insuffisante en oligo-éléments, due à un défaut d’apport soit en qualité soit en quantité.
- Les carences secondaires, qui font suite à la consommation d’un élément qui inhibe l’absorption d’un oligo-élément (Arthington, 2003).
Par la suite, il convient donc de s’intéresser aux pratiques pouvant conduire à des carences primaires et/ou secondaires.
Identification des pratiques à risque de mauvaise assimilation
Les pratiques à risque de mauvaise assimilation correspondent aux pratiques conduisant aux carences secondaires.
Les carences secondaires en cuivre sont relativement fréquentes. Notamment lors d’interactions avec le molybdène, le soufre, ou encore le fer. Les deux premiers éléments inhibent l’absorption du cuivre par captation et complexation du cuivre, formant ainsi des molécules très peu absorbées dans l’intestin et peu biodisponibles. Lorsque les bovins pâturent dans des prairies où l’herbe est trop rase, l’ingestion de terre, dont le fer peut représenter jusqu’à 10% de matière sèche, peut-être à l’origine d’une carence en cuivre (Guerin, 2010). Un excès de soufre, parfois présent dans l’eau par exemple, inhibe aussi l’absorption de sélénium. Ainsi, l’utilisation d’un puit de forage, recueillant les eaux de pluie, ou l’application d’engrais riche en souffre sur les cultures sont deux pratiques à risque de carence en cuivre et en sélénium (Arthington, 2003).
Tout phénomène à l’origine d’une altération du transit digestif peut être à l’origine d’une carence secondaire en oligo-éléments, par baisse de son absorption digestive. Ainsi par exemple, une diarrhée chronique non traitée peut être à l’origine de carences (Graham, 1991).
Identification des pratiques à risque de mauvaise complémentation
La très grande majorité des fourrages est carencée en oligo-éléments, on comprend donc que l’absence de complémentation minérale représente une pratique à risque de carence importante (Rollin, 2002).
Cependant, dans la plupart des travaux de nutrition animale, la majorité des recherches portent sur les éléments majeurs de la ration tels que les protéines digestibles, l’énergie ou encore la matière azotée ; puis dans un second temps sur le calcium et le phosphore et enfin, peu d’entre elles portent sur les oligo-éléments. Les recommandations dans ce domaine se limitent donc souvent à l’utilisation d’un produit commercial contenant des oligo-éléments. Cependant, ce produit ne doit pas représenter un coût trop important tout en étant de bonne qualité, c’est-à-dire être suffisamment biodisponible pour les bovins (Adams, 1975; Meschy, 2010).
Evaluation des formes d’apport en oligo-éléments
Les galéniques disponibles
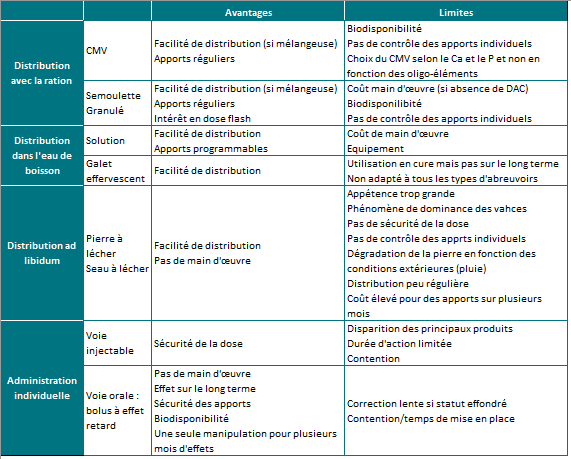
Dans un second temps, il est intéressant de savoir quel est le mode de distribution et si les apports sont plutôt maitrisés, avec un mode de distribution individuel et mesuré, ou plus aléatoires, avec une mise à disposition ad libidum des minéraux. Le tableau ci-dessous reprend les différentes formes macroscopiques disponibles pour les éleveurs. Lors de la mise en place d’une complémentation et notamment lors du choix de la forme galénique, il est important de considérer aussi la taille du troupeau, le type de bovins (laitiers/allaitants) et les contraintes en termes de temps et main d’œuvre pour l’éleveur. En effet, une complémentation par voie indirecte (eau de boisson, mélange à la ration) est souvent préférable à une absence de complémentation, bien que les apports individuels soient moins bien précisément connus (Meschy, 2010).
La forme et la fréquence des apports en oligo-éléments influencent fortement leur biodisponibilité. Cette dernière notion correspond à la proportion effectivement active dans l’organisme et métabolisée par rapport à la quantité d’élément absorbée. Cela correspond donc à la partie valorisée de la ration, pour les oligo-éléments.
Ainsi, l’excrétion des oligo-éléments augmente lorsque les apports augmentent. Si on prend l’exemple de minéraux distribués avec la ration, les quantités apportées sont relativement importantes pour pouvoir couvrir les besoins, mais la fréquence est faible : seulement deux fois par jour. Les mécanismes d’absorption sont alors rapidement saturés et une partie non négligeable des apports est directement éliminée.
Même si la quantité distribuée semble suffisante pour répondre aux besoins des animaux, la quantité absorbée est trop faible – du fait du mode de distribution. A l’inverse, une même quantité distribuée sur une durée plus importante, comme des dispositifs à libération continue par exemple, sera mieux absorbée par l’animal et donc mieux valorisée (Spears, 2014).
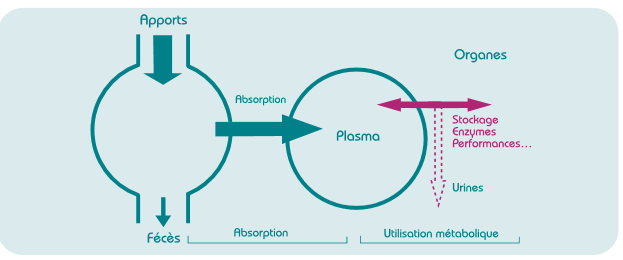
On comprend ainsi que la quantité d’oligo-éléments apportée dans la ration n’est pas une donnée suffisante. De plus, la biodisponibilité d’un élément suppose que celui-ci a été non seulement absorbé, mais aussi transporté jusqu’au tissu cible et qu’il y a effectué son action. Or, des interactions existent entre les différents composants de la ration et la vitesse du transit, l’état du tube digestif, le stade physiologique de l’animal sont parmi les facteurs influençant l’absorption des éléments par la barrière intestinale. La notion d’utilisation métabolique (figure ci-dessous) permet de décrire les apports, l’absorption, la biodisponibilité, le métabolisme et l’élimination des oligo-éléments (Arnaud & Belleville-Nabet, 1995).
La solubilité des oligo-éléments est un autre paramètre important influençant leur biodisponibilité. Celle-ci varie avec la forme biochimique apportée, et peut influencer sur les durées de délitement des dispositifs à effet retard.
Les formes chimiques d’apport
Nous avons rappelé les différentes formes macroscopiques sous lesquelles se trouvent les oligo-éléments. Cependant, bien que cette forme ait une grande importance dans la biodisponibilité des éléments minéraux, il ne faut pas oublier de prendre en compte leur forme chimique. En effet, toutes les sources d’oligo-éléments ne peuvent être exploitées de manière identique par les animaux : elles peuvent être totalement assimilées et utilisées par l’animal, partiellement, ou totalement éliminées, faisant ainsi varier leur biodisponibilité (McDowell 2003).
Il existe de nombreuses formes chimiques d’apport en oligo-éléments, qui peuvent être réparties en deux groupes : les sels inorganiques et les sels organiques. Depuis la fin des années 90, une troisième catégorie existe : les hydroxy oligo-éléments.
Les sels inorganiques
Il s’agit d’un élément minéral et d’un ligand non-carboné. Ce sont les premières formes mises mis sur le marché, dans les années 50. Ce groupe est constitué de :
- Sulfates (SO42-)
- Chlorures (Cl-)
- Carbonates (CO3-)
- Oxydes (O2-)
Parmi ces formes inorganiques, les sulfates sont les plus assimilables pour les animaux. Les sels inorganiques sont largement utilisés de nos jours, à la fois pour prévenir les carences, mais aussi comme solution curative lorsque la carence est avérée. Les bactéries du rumen exercent une action forte sur la dégradation et l’absorption des carbonates et des oxydes. La pureté, variable selon les sources de minéraux utilisées, est un élément important influençant la biodisponibilité d’un élément. Par ailleurs, la biodisponibilité des sels inorganiques peut être fortement impactée par la présence de substances antagonistes, diminuant ainsi le métabolisme de certains éléments. Moins sensibles à ces interactions, les formes organiques sont souvent préférées car la biodisponibilité est alors plus importante, malgré un prix un peu plus élevé (Spears, 2013).
Les sels organiques
Un sel organique est composé d’un élément minéral et d’un ligand carboné. Ce sont soit des complexes, synthétisés artificiellement, entre des éléments organiques et les ions métalliques, soit des complexes produits par des levures. Ils ont été développés dans les années 70, en complément des formes inorganiques, afin d’améliorer la biodisponibilité. On y retrouve :
- Des protéinates, complexes entre acides aminés et ion métallique,
- Des chélates d’un seul acide aminé avec un ion métallique,
- Des complexes polysaccharidiques,
- Le malate, le fumarate et le citrate, mais ils sont très peu employés en alimentation animale car très chers,
- Les levures sélénisées, uniquement pour le sélénium.
L’objectif principal d’une supplémentation sous forme organique est d’augmenter la biodisponibilité des oligo-éléments apportés. Cela serait permis par la liaison covalente entre le ligand et l’élément minéral, car celle-ci confèrerait au composé minéral, une meilleure résistance dans le tube digestif.
Les formes hydroxyanalogues
Un hydroxy oligo-élément est composé d’un élément minéral, lié à un groupement hydroxyle et un groupement chlorure par des liaisons covalentes. Ce sont des éléments normalement insolubles dans l’eau, ils sont donc non hygroscopiques et moins réactifs que les sulfates. Par ailleurs, en améliorant la biodisponibilité des oligo-éléments, les quantités rejetées dans l’environnement via les fèces sont moins importantes. De même, leur très faible solubilité au pH du rumen, permet de réduire l’impact sur la flore ruminale. En effet, les besoins en oligo-éléments des bovins sont supérieurs à ceux de leur flore ruminale mais des concentrations trop élevées, en zinc et en cuivre notamment, peuvent être à l’origine d’une détérioration de la flore ruminale ((Intellibond), 2013).
Le type de sel utilisé ne conditionne pas seulement la biodisponibilité de l’oligo-élément. Par exemple, la forme organique ou inorganique d’apport conditionne la vitesse de délitement des bolus d’un point de vue galénique. Un bolus construit majoritairement à base de sels organiques aura une durée de délitement plus rapide qu’un bolus construit majoritairement à base de sels inorganiques.
L’idée est donc de trouver un compromis entre durée de délitement/action souhaitée et composition, par les fabricants.
Évaluation du statut en oligo-éléments des animaux
Évaluer l’assimilation par les bovins des oligo-éléments de leur ration permet d’évaluer les apports effectifs de la ration. Le statut en éléments traces peut être obtenu grâce à différents prélèvements : sang, lait, salive ou encore tissus animaux.
Prélèvement sanguin
Le statut sanguin en oligo-élément peut être obtenu de plusieurs manières :
- Directe, par mesure des concentrations plasmatiques des éléments,
- Indirecte en évaluant l’activité de certaines enzymes ou hormones dont le fonctionnement et la concentration dépendent d’oligo-éléments particuliers,
- Indirecte en mesurant les concentrations de certains métabolites qui s’accumulent lors de carences (tableau ci-dessous : Éléments de mesure indirecte du statut en oligo-éléments d’après Herdt & Hoff 2011)
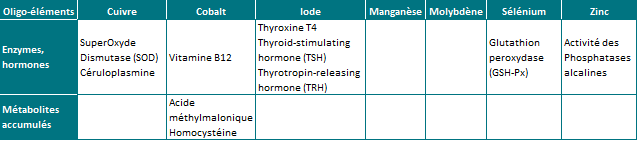
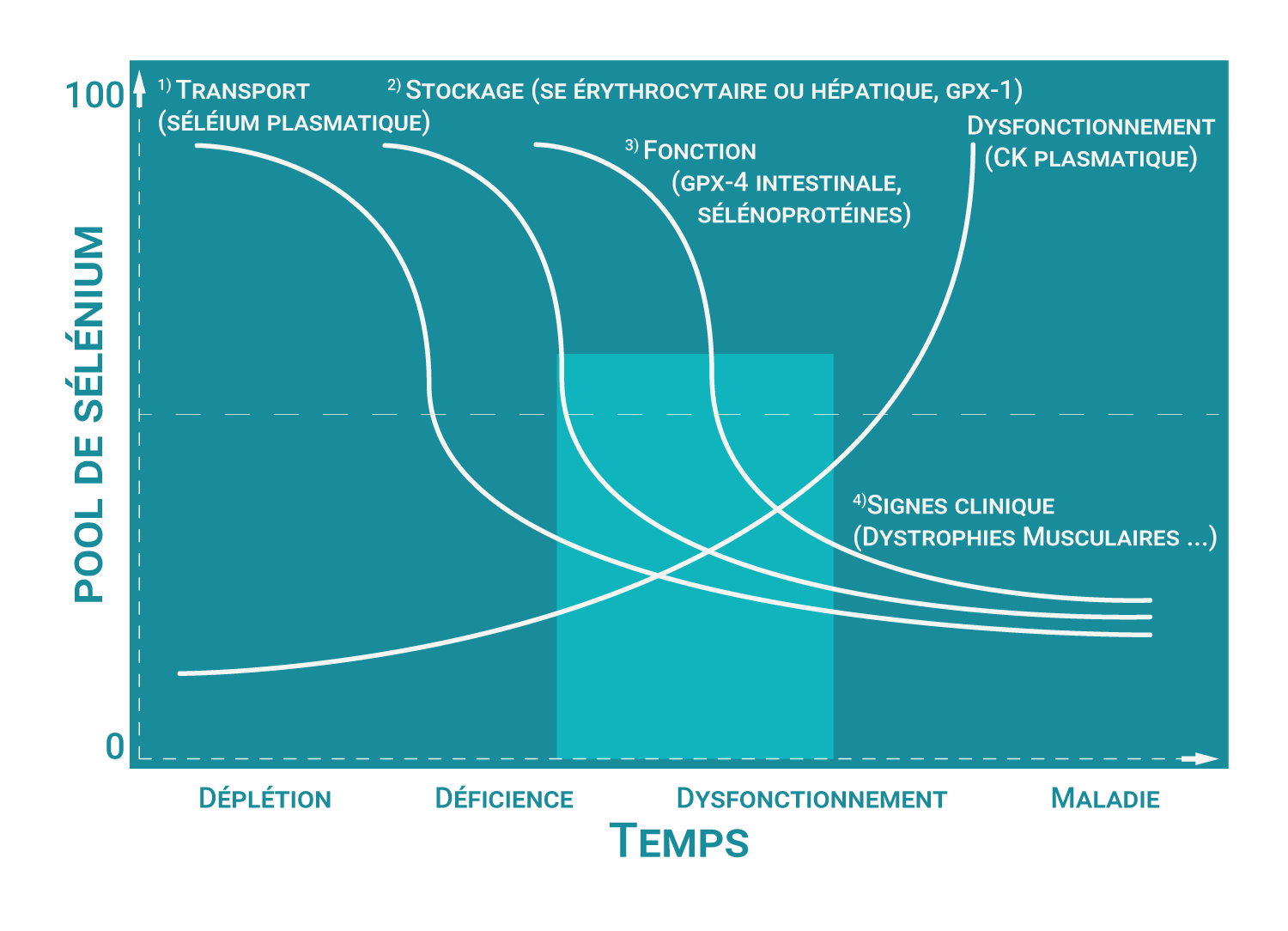
La mesure indirecte n’est cependant possible que lorsque les signes cliniques sont présents, c’est-à-dire que la carence est relativement importante (figure ci dessous). Actuellement, les éleveurs veulent de plus en plus identifier les carences lorsqu’elles sont subcliniques et avant qu’elles n’aient un impact économique. Ces mesures indirectes ne sont alors plus suffisantes. Par ailleurs, ce type démarche nécessite une technique d’analyse différente pour chaque oligo-élément, ce qui se traduit par un prix significativement plus élevé que si on mesurait les concentrations plasmatiques totales en oligo-éléments.
La mesure des concentrations plasmatiques en oligo-éléments est la méthode de référence et la plus souvent employée car la plus facile à mettre en œuvre d’un point de vue pratique. C’est aussi une méthode standardisée et donc facilement répétable. De plus, les dernières avancées techniques, comme le dosage par torche à plasma couplée à la spectrométrie de masse (ICP/MS), ont permis de réduire les coûts pour l’éleveur, d’obtenir des résultats rapides et précis (Chappuis & Poupon, 1991; Lumet & Negriolli, 2007). Cependant, il a été montré que les concentrations plasmatiques en oligo-éléments pouvaient être influencées par les apports alimentaires, l’homéostasie, le stade physiologique ou encore l’âge (Herdt & Hoff, 2011).
Lorsque l’objectif est d’établir le profil plasmatique en oligo-éléments de l’élevage, il est important de choisir des animaux au hasard dans les élevages, mais qui soient les plus représentatifs du troupeau. En effet, cela augmente la puissance des valeurs prédictives des analyses et la sélection au hasard permet d’atténuer les variations individuelles, notamment celles liées au stade physiologique (Herdt, 2000; Siliart, 2014). Cependant il ne faut pas les prélever trop jeunes, moins de 2 mois, ni dans le mois péri-partum, car les variations en minéraux au cours de ces périodes sont très importantes et non représentatives du statut global du troupeau. De plus, les animaux prélevés doivent être sains cliniquement, car les statuts en oligo-éléments sont très influencés par différentes pathologies – par exemple les concentrations sériques en cuivre augmentent lors de processus inflammatoires (Herdt & Hoff, 2011).
Le nombre optimal d’animaux à prélever correspond à 10% de l’effectif de l’élevage, mais il dépend de l’objectif de l’analyse : estimer les concentrations moyennes en oligo-éléments de l’élevage, évaluer la prévalence d’une carence ou seulement la mettre en évidence. Le nombre minimum d’animaux à prélever varie donc selon les auteurs entre 4 et 12 (Herdt & Hoff, 2011; Kincaid, 1999; Oetzel, 2004). Pour diminuer les frais, on peut parfois réaliser des pools d’échantillons de sang de plusieurs animaux. On peut alors prélever entre 5 et 20 animaux selon les auteurs, et comparer la moyenne du groupe aux valeurs de référence de ce groupe. Cependant, lors du dosage de la glutathion peroxydase pour l’évaluation du sélénium, le nombre d’individus prélevés serait de 5 maximum. Au-delà, la valeur obtenue pour le mélange serait statistiquement trop différente de la valeur moyenne des individus (Pitel, Besnier, Reisdorffer, Defontis, & Richard, 2014). Cependant, l’utilisation de pools d’échantillons pour évaluer le statut d’un élevage est soumis à controverse. En effet, une analyse de sang de mélange masque les hétérogénéités de statuts entre les animaux. De plus, une seule valeur extrême peut modifier de façon significative les résultats. On ne pourra donc interpréter que des résultats très hauts ou très bas (Guyot & Rollin, 2007; Siliart, 2014).
Enfin, lors de prélèvements sanguins, il est important de choisir le bon tube de prélèvement. En effet, les tubes en verre ou ceux avec un bouchon en caoutchouc risquent de contaminer l’échantillon, en favorisant l’hémolyse ou en augmentant artificiellement le taux de zinc. Il est conseillé de prélever sur des tube EDTA K2, traités spécifiquement au niveau du bouchon pour permettre le dosage des oligo-éléments.
Ces tubes sont fournis par Vétalis à tous les vétérinaires qui en font la demande.
Prélèvement de tissus
Ces prélèvements permettent un accès aux différents organes de stockage des oligo-éléments. Ainsi, la biopsie de foie donne une évaluation directe des réserves en cuivre, en fer et en cobalt. Bien que ce prélèvement soit relativement facile et rapide à réaliser, il reste plus cher et plus lent qu’une prise de sang, c’est pourquoi il est souvent peu utilisé en Europe.
Lors d’une période de jeûne prolongé, un stress ou encore des phénomènes inflammatoires ou infectieux – même débutants – les quantités d’oligo-éléments stockés sont modifiées, et ce, avant l’apparition de tout signe clinique ou de toute variation des concentrations plasmatiques (Suttle, 2010). C’est pourquoi, lorsque le prélèvement est possible, les biopsies peuvent être intéressantes à réaliser – d’autant plus dans un contexte clinique (Herdt & Hoff, 2011). Enfin, une exposition chronique à de fortes doses de minéraux entraine leur accumulation dans les organes de stockage, le plus souvent sans augmentation de leurs concentrations plasmatiques. Les biopsies permettent alors d’objectiver l’intoxication avant que les conséquences cliniques ne se déclarent (Auza, 1983).
Prélèvement de lait
Pour l’iode et le sélénium, les quantités excrétées dans le lait sont le reflet du statut à court terme de l’animal. L’analyse peut porter sur un seul individu ou sur le lait de tank. Il faut toutefois être sûr que du lait contaminé par des érythrocytes n’a pas été mis dans le lait de mélange, ce qui fausserait la valeur du sélénium (Guyot, Saegerman, Lebreton, Sandersen, & Rollin, 2009).
Cependant, l’iode ne peut pas être dosé sur le colostrum car celui-ci contient trois à cinq fois plus d’iode que le lait. De plus, lors de l’utilisation de produits de traite iodés, ce dosage est inutile car les produits augmentent artificiellement le taux d’iode mesuré (Meschy, 2010).
Autres prélèvements
Les profils urinaires et pilaires peuvent paraître intéressants car ils sont facilement réalisables par un grand nombre de personne. Cependant ce ne sont pas les prélèvements les plus pertinents. En effet, les concentrations urinaires en oligo-éléments ne sont pas proportionnelles aux concentrations sanguines : lorsque les apports alimentaires augmentent, l’élimination urinaire augmente aussi. De plus, l’excrétion urinaire dépend de l’oligo-élément et de la forme d’ingestion, par exemple l’élimination rénale du sélénium est augmentée lorsque celui-ci est apporté sous forme inorganique par rapport à un apport sous forme organique. De manière générale, lorsqu’aucune lésion rénale n’est présente, les éléments traces urinaires proviennent d’un apport excessif ou d’un amaigrissement brutal (Guyot & Rollin, 2007; Siliart, 2014).
Les concentrations pilaires varient fortement selon la couleur : les poils noirs sont plus riches en zinc, les poils rouges sont plus riches en cuivre. De plus, ces concentrations sont des indicateurs très tardifs d’une éventuelle carence. Enfin, les poils sont très souvent contaminés par le milieu extérieur (lors de frottements au cornadis par exemple) et les poussières. Les concentrations pilaires en oligo-éléments dépendent donc plus de la couleur du poil, de l’âge de l’animal et du milieu extérieur que de son statut (Meschy, 2010; Siliart, 2011, 2014).
Ainsi ni les prélèvements d’urine ou de poils ne sont adaptés pour évaluer le statut en oligo-éléments des bovins.
 Contact
Contact Export
Export